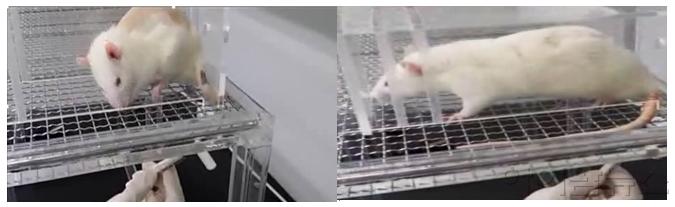
 ▲ 통증 측정실험 von freyfilament: 신경병증성 모델(SNI)에서 통증이 유발된 실험용 쥐(왼쪽)에게 자극을 주었을 때 움추려드는 모습과 KLS-2031 투여 후 정상적으로 통증자극을 인식하는 실험용 쥐(오른쪽)의 모습
▲ 통증 측정실험 von freyfilament: 신경병증성 모델(SNI)에서 통증이 유발된 실험용 쥐(왼쪽)에게 자극을 주었을 때 움추려드는 모습과 KLS-2031 투여 후 정상적으로 통증자극을 인식하는 실험용 쥐(오른쪽)의 모습
[아이팜뉴스] 코오롱생명과학(대표 이우석)은 신경병증성 통증 유전자 치료제인 ‘KLS-2031’의 미국 1상/2a상 임상 진행을 위한 FDA의 IND 승인이 완료했다고 11일 밝혔다.
KLS-2031은 세계 최초 골관절염 세포 유전자 치료제인 ‘인보사’의 후속 파이프라인으로 기존 신경병증성 통증 치료 방식과는 달리 유전자를 이용한 주사요법의 치료제다. 인보사 출시 이후 유전자 치료 전문기업으로 거듭나기 위한 새로운 도전이 시작될 것으로 보여진다.
신경병증성 통증이란 신체의 손상이 아닌 신경계의 손상이나 기능적 이상으로 발생하는 통증을 말한다. 난치성이고, 만성적으로 오래 지속되는 특성이 있으며, 일반인의 경우 통증으로 느끼지 못하는 자극이지만 환자들에게는 극심한 고통을 주는 감각신경계 질환이다.
KLS-2031은 2개의 ‘아데노부속바이러스 전달체(AAV vector)’에 3개의 치료 유전자(GAD65, GDNF, IL-10)를 탑재한 유전자 치료제다. 첫 번째 전달체에는 GAD65 유전자를 탑재해 뇌로 가는 통증 신호를 억제하는 작용을 하며, 두 번째 전달체에는 GDNF와 IL-10유전자를 탑재해 각각 손상된 신경을 보호하고 염증을 막는 작용을 하게 된다.
이를 통해 통증 완화효과를 기대할 수 있게 된다. 시술방식은 1회 국소주사로 진통 효능이 장기간 지속되도록 개발됐으며, 기존의 치료제로는 효과를 보지 못하는 신경병증성 통증을 겪고 있는 환자들을 타깃으로 하고 있다.
코오롱생명과학이 미국에서 진행할 이번 1상/2a상 계획은 미국 2개 임상기관을 통해 안전성 및 유효성 평가를 목적으로 올해 내에 임상을 개시할 예정이며, 시험대상은 18명으로 투약 후 24개월 관찰을 할 계획이다.
KLS-2031 연구는 유전자 치료제 분야 등 국내 기업의 글로벌 도약을 위해 보건복지부 및 과학기술정보통신부가 공동출연해 2015년부터 3년간 지원하는 ‘글로벌 첨단 바이오의약품 기술개발사업 과제 지원’으로 수행됐다.
코오롱생명과학의 이우석 대표는 “세계 최초 골관절염 유전자 치료제인 인보사의 성공적인 상업화 이후 후속 파이프라인으로 연구개발 중인 KLS-2031의 미국 FDA의 임상 승인은 코오롱생명과학이 글로벌 시장에서 유전자 치료 전문기업으로 인정받고, 국내의 최첨단 유전자 연구수준을 해외 바이오시장에 한층 더 알릴 수 있는 긍정적인 기회가 될 것”이라고 밝혔다.
 ▲ 통증 측정실험 von freyfilament: 신경병증성 모델(SNI)에서 통증이 유발된 실험용 쥐(왼쪽)에게 자극을 주었을 때 움추려드는 모습과 KLS-2031 투여 후 정상적으로 통증자극을 인식하는 실험용 쥐(오른쪽)의 모습
▲ 통증 측정실험 von freyfilament: 신경병증성 모델(SNI)에서 통증이 유발된 실험용 쥐(왼쪽)에게 자극을 주었을 때 움추려드는 모습과 KLS-2031 투여 후 정상적으로 통증자극을 인식하는 실험용 쥐(오른쪽)의 모습


 위로
위로 목록
목록